El científico del CONICET Daniel Alonso participó del desarrollo de esta iniciativa, que busca ser un aporte para el desarrollo de nuevas estrategias terapéuticas contra tumores en humanos. La nueva herramienta ya fue utilizada en un trabajo publicado en Nature que aborda las relaciones específicas entre un importante oncogén y el desarrollo de cáncer en diferentes tejidos
El científico del CONICET Daniel Alonso participó del desarrollo de esta iniciativa, que busca ser un aporte para el desarrollo de nuevas estrategias terapéuticas contra tumores en humanos. La nueva herramienta ya fue utilizada en un trabajo publicado en Nature que aborda las relaciones específicas entre un importante oncogén y el desarrollo de cáncer en diferentes tejidos
Un equipo científico internacional, del que participa el investigador del CONICET Daniel Alonso, director del Centro de Oncología Molecular y Traslacional (COMTra-UNQ), acaba de dar a conocer el primer atlas de líneas celulares de cáncer de ratón (Mouse Cancer Cell line Atlas). Esta valiosa herramienta, útil para entender cómo se desarrollan y se pueden tratar diferentes tipos de cáncer en humanos, tiene como primer fruto un trabajo publicado en la prestigiosa revista Nature, en el que se analizan las relaciones específicas entre el gen KRAS (que aparece mutado en muchos tipos de cáncer) y el desarrollo de tumores en distintos órganos.
 Los modelos en ratón de cáncer y otras enfermedades se han convertido en recursos indispensables y una fuente de descubrimientos clave para entender sus mecanismos de acción, así como para el desarrollo de nuevos tratamientos.
Los modelos en ratón de cáncer y otras enfermedades se han convertido en recursos indispensables y una fuente de descubrimientos clave para entender sus mecanismos de acción, así como para el desarrollo de nuevos tratamientos.
En este sentido, el nuevo Atlas es una colección curada de líneas celulares de cáncer en ratones, con casi 600 ejemplares, que cubren decenas de tipos de cáncer, incluyendo todos los más prevalentes. Conforma una enorme base de datos abierta, accesible para científicos de todo el mundo, con información genética completa, estudios histopatológicos, inmunológicos y análisis comparativos con los tumores homólogos en el ser humano.
“Hasta ahora, si bien había colecciones de líneas celulares humanas, no existía un recurso de estas características para el cáncer en el ratón, que es el modelo experimental más utilizado en investigación biomédica y el que mejor reproduce la enfermedad en los seres humanos”, señala Alonso.
El desarrollo del Atlas fue liderado desde Alemania por los científicos Sebastian Mueller y Roland Rad, de la Escuela de Medicina y Salud de Munich y el Centro de Investigación en Cáncer de Heidelberg, quienes reunieron la colección de líneas celulares convocando a investigadores de otros centros de Alemania, Reino Unido, Canadá, Estados Unidos, España, Italia y Argentina.
“Mi aporte incluyó una línea celular de un cáncer agresivo, que aislamos hace más de tres décadas durante mi tesis doctoral junto a la investigadora Elisa Bal en el Instituto Oncológico Roffo (UBA) y validamos como modelo durante todos estos años en la Universidad Nacional de Quilmes (UNQ). Me desempeño como el contacto en Latinoamérica de esta iniciativa internacional”, afirma Alonso.
El oncogén KRAS en distintos cánceres
En el estudio publicado recientemente en Nature (del cual Alonso también es uno de los autores), se utilizó el atlas como una herramienta para estudiar la evolución específica de los cánceres en cada tejido bajo impulso del oncogén KRAS.
Los oncogenes son genes que se alteran en las células cancerosas, dando como resultado una proteína alterada que estimula de manera excesiva el crecimiento de esa célula. Los oncogenes RAS, y particularmente el KRAS, son los más frecuentemente afectados en el cáncer humano. No obstante, cuando se produce un cáncer son varios los genes que se alteran en la misma población celular para dar lugar a la enfermedad y la evolución es muy variable en cada tejido.
“Los oncogenes como KRAS muestran una gran especificidad según el tejido en el que actúan; su capacidad para causar cáncer, las interacciones genéticas y los efectos en las células varían mucho, pero las razones detrás de esto aún no están del todo claras. De alguna forma, los vínculos precisos entre el oncogén mutado y la progresión del cáncer, hasta los complejos cambios en el comportamiento celular que llevan a cáncer en un tejido, pero no en otros, constituyen un ’eslabón perdido’ para abordar mejor la prevención y el tratamiento”, indica Alonso.
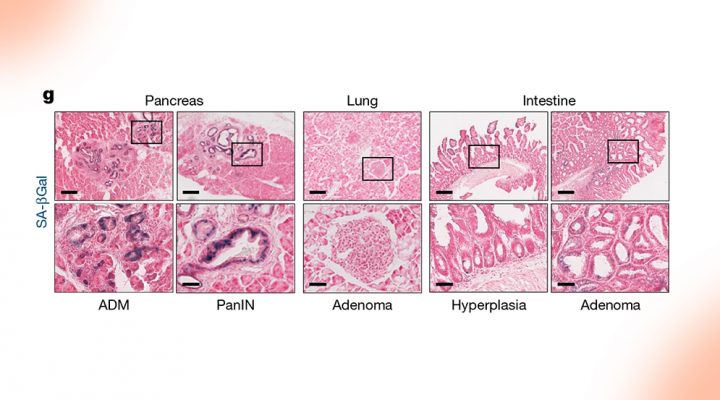
El estudio permitió analizar estas cuestiones en tipos de cáncer fuertemente asociados al oncogén KRAS, como pancreático, pulmonar e intestinal. “Además, al empezar a entenderse estos procesos evolutivos en estas líneas celulares de ratón, el propio modelo estudiado es un ‘banco de pruebas’ para avanzar hacia nuevos enfoques terapéuticos para el cáncer humano. De hecho, parte del estudio buscó el paralelismo de los resultados con datos clínicos”, indica el investigador del CONICET.
Aunque normalmente, las personas tienen en su ADN dos copias o alelos de cada gen (una por parte materna y otra por parte paterna) las mutaciones en KRAS pueden provocar que las copias de este gen se multipliquen en las células afectadas. En este sentido, el estudio muestra, entre otras cuestiones, que este aumento en la cantidad de copias genéticas de KRAS mutado tiene efectos específicos según el tipo de célula y eso determina cuándo puede surgir un cáncer en cada tejido. En caso del páncreas, el aumento causa una “reprogramación” del comportamiento celular muy al inicio de la transformación cancerosa. En el tejido intestinal, se observa un bloqueo temprano de la especialización celular, que genera las condiciones para la generación de otras mutaciones que colaboran con el oncogén KRAS.
“De manera más general, estos hallazgos empiezan a echar luz sobre los factores innatos y adquiridos que guían la evolución de un cáncer en distintos tejidos, pudiendo eventualmente establecerse patrones moleculares y dinámicas temporales más predecibles, con resultados esperables en el compartimiento celular. Es un avance importante hacia una comprensión mecanicista de los siempre complejos e inestables genomas cancerosos”, concluye Alonso.
De acuerdo con el investigador, uno de los próximos objetivos del grupo es promover el uso de la plataforma que ofrece el Atlas y seguir reuniendo voluntades desde todos los rincones del mundo, para continuar develando en todos los tipos de tumores las brechas de conocimiento que aún persisten.
Referencia bibliográfica:
Mueller, S., de Andrade Krätzig, N., Tschurtschenthaler, M. et al. A disease model resource reveals core principles of tissue-specific cancer evolution. Nature (2026). https://doi.org/10.1038/s41586-026-10187-2
Por Miguel Faigón